アルツハイマー型認知症 (Alzheimer-type dementia: ATD) の病理
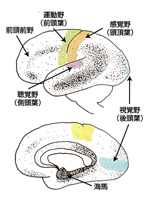
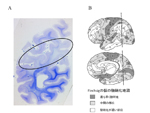
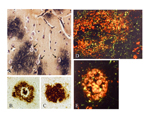
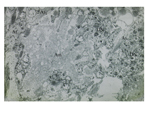
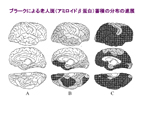
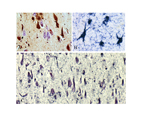
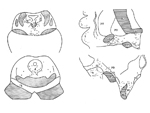
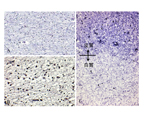
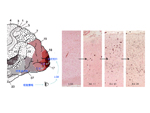
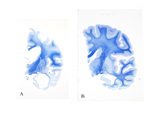
ATDの約60%は記憶障害を初発症状として始まる。これはATDでは海馬領域から病変が始まることに対応している。ATD病変は大脳辺縁系を経て大脳皮質に広がるが、よく知られているように一次運動・感覚野は末期に至るまで比較的に保たれるのに対して、連合野が冒されやすい。連合野の冒され方も一様ではない。図1はATDの病変領域図であるが、図に示されているように通常は道具的機能を担った脳の後方領域に病変が強い。ATDの連合野では、後部帯状回と上頭頂小葉が最初に冒され、次いで、下頭頂小葉、中・下側頭葉が続く。経時的な機能画像研究で示されているように、ATD病変は後方から前方(前頭葉)に広がってゆく。早期に冒される新皮質の中でも最も病変が高度に及ぶのは後部帯状回と下頭頂小葉である。最も強く冒される下頭頂小葉は角回、縁上回で構成される。実際の臨床でもATDでは記憶障害に次いで、物を使うことが困難になったり、空間認知の障害が現れたり、言語や概念の障害が現れる。前額断の脳標本で見ても頭頂連合野のなかでも上位に位置する領域が強く冒されていることが分かる (図2A)。この領域はFlechsigの脳地図(図2B)では髄鞘化の最も遅い領域である。すなわち、ATDの頭頂連合野は最も遅くに成熟し、ヒトで最も高度に発達した領域から冒される傾向がある。機能面からみると異なる感覚情報を整理統合し、受動的な知覚・認知機能を担う領域(後部異種感覚連合野)から冒され、これらの情報に基づいて能動的に状況を判断したり、計画を立てたりする遂行機能や意欲に関与する領域(前部異種感覚連合野)に及んでくる。但し、必ずしも上述したような一般的な過程を示さない場合もあり、前頭葉から病変が始まったという症例報告もある。それでは時間経過を念頭にもう少し詳しくATDの病理をみて行こう。 ATDでは20〜30年という長い潜伏期間を経て、認知症が発現すると言うことが定説となっているが、顕微鏡下で最初に捉えられる所見はどの領域にどのように始まるのであろうか? ATD脳で起こる主要な病理所見は老人斑(senile plaque: SP)と神経原線維変化(neurofibrillary tangle: NFT)の大量の出現とニューロンの脱落で、これに組織の反応、清掃と修復像が加わってATDの病理像が形成される。アミロイドカスケード仮説(図3)によれば、最初にアミロイドβ(Aβ)沈着が起こり、次いでNFTが形成され、最後に神経細胞脱落が起こるとされている。この仮説に従えば最初に起こる現象はAβ沈着である。 生理的加齢性変化の項で述べたように、SPは加齢に伴って増加し、分布の範囲が広がって行くが、生理的加齢とATDの間に明確な境界はなく連続している。SPは最初に前頭葉や側頭葉の底面の皮質第3層を中心に出現し始める。年齢で見ると30歳代でSPが出現することは稀であるが、40歳代で一部のヒト(約8%)に出現が認められる。この頻度は加齢とともに増加してゆき、非認知症者で見ると、50歳代で約16%、80歳代になると約60%のヒトの脳に出現している。最初に出現するSPのタイプはび漫性老人斑(diffuse plaque: DP)である。DPは不整形で、しばしば神経細胞がその中に散在しているが、神経細胞が傷害されているようには見えない(図4A)。免疫二重染色を施した厚切り切片を共焦点レーザー顕微鏡で観察すると、DPを軸索が傷害されることなく横切っていることが分かる(図4D)。この段階のDPを電子顕微鏡で観察すると、線維形成に乏しいアモルファスなAβ陽性構造物が観察される。この構造物は細胞膜から出ているAβであることが知られている。一部にアミロイド線維が混在するようになるとグリコーゲン顆粒で満たされたアストロサイトの突起の反応が見られるようになる。電子顕微鏡で形態を観察した限りではアミロイド線維形成がない段階では組織の反応は乏しいが、線維形成が始まると異物として認識され、組織の反応が始まるように見える。SPは量的な増加と空間的な広がりとともに、出現するタイプも形を変えて行き、定型老人斑(typical plaque: TP, 図4B,E)や原始老人斑(primitive plaque: PP, 図4C)と名付けられた密なアミロイド線維から成るタイプが非認知症であっても増えて来る。TPを前述の共焦点レーザー顕微鏡で観察するとアミロイド塊に加えて断裂して腫大した軸索(dystrophic neurute: DN)が混在して観察される(図4E)。DNには多数のミトコンドリアやdense bodyに満たされたものや、NFTを構成するpaired helical filament (PHF)が認められる*。DNに加えて、ミクログリアやアストロサイトの突起がアミロイド塊を取り巻いてSPを形成している(図5)。このように線維化したAβ塊は組織の反応としてのミクログリアやアストロサイトや腫大した軸索で周囲を取り巻かれており、その過程で軸索は断裂・腫大するので組織が傷害される。
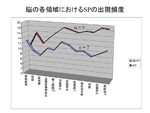
このように時間をかけて、よりアミロイド密度の高いタイプのSPへ置き換わって行くとともに、出現領域の広がりとともに密度も増加し(図6)、ATD病理学的な診断基準を満たす状態となる。
* DNはNFTが細胞外に放出されたghost tangleの周囲にも形成され、その形態はSPに見られるものと同じでPHFを伴っているし、DNに加えてミクログリアやアストロサイトの突起も観察される。アミロイド線維もNFTもβシート構造を示す点で共通している。 アミロイドカスケード仮説では神経原線維変化 (neurofibrillary tangle: NFT, 図7) はAβの蓄積に続いて形成される(図3)とされるが、これは主にATD脳の大脳新皮質に当てはまる現象のように見える。NFTは認知症のない人にも出現し、生理的加齢に伴って最初に海馬領域に出現して増加するが、大脳新皮質では前頭葉底面や側頭葉の内側部にごく少数出現するのみである。SP(Aβ)の存在がなければ加齢が進んでもNFTは辺縁系に留まって新皮質に広がらないように見える*。
これは次のように解釈される。異常にリン酸化したタウの蓄積は亜急性硬化性全脳炎(SSPE)や進行性多巣性白質脳症(PML)のようにウイルスが長期に渡って細胞内に存在したり、ボクサー脳のように頭部への衝撃が繰り返されたり、さらには線維性グリオーシスの強い領域に出現するタウ陽性アストロサイトなどのように、広くストレスの加わる条件下で起こる細胞反応と考えられ、新皮質のSPにも当てはまる。すなわち、老人斑(Aβ沈着)の存在下でNFT形成が促進されると考えられる。
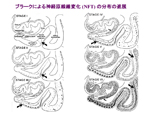
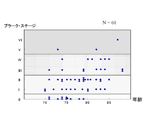
生理的加齢性変化の項で述べたようにNFTも加齢性構造物の一つである。最初のNFT形成は60歳代に経嗅内野に始まり、嗅内野を経て海馬支脚、さらにアンモン角のCA1、さらにはCA3, 4へと加齢と伴に広がって行くがCA2は免れる。CA2は虚血性変化に対して強い部位(抵抗帯と呼ばれる)であるが、加齢性変化にも抵抗性がある。海馬領域のNFT形成は生理的加齢とATDで連続性があり、ATDの進行でNFT形成も進行する。このようなNFTの辺縁系での進展はNFTのブラークステージ(BS)の図に示されている(図8:Braak H and Braak E, Acta Neuropathol 82(1991)239-259)。図9は総合病院で死亡した高齢者剖検例のBSを調べたもので、ほぼ一般の高齢者の構成を反映していると考えられるが、加齢とともにBSは右肩上がりに増加するが、個人差も大きいことが分かる。
ブラークステージの図には示されていないが、加齢に伴って皮質下神経核では扁桃体の特に皮質内側核群(発生的に古い核群)、マイネルト核、対角回核や脳幹領域の背側被蓋核、青斑核、縫線核群(上中心核)などのモノアミン神経核にもNFTが散見される。これらの諸核はATDでもNFTの好発神経核である。とくにマイネルト核は抗認知症薬のアセチルコリンエステラーゼ阻害薬と関連した神経核であるが、NFTの出現頻度で見るとATDの初期においては約10〜20%程度、進行した段階では60%以上、失外套状態に陥った最末期ではほぼ100%、すなわち、残存しているのはghost tangleとなったNFTのみという状態となる。ATDが進行するとマイネルト核のみならず投射先の大脳皮質の神経細胞脱落も進行するので、抗認知症薬(アセチルコリンエステラーゼ阻害薬)の効果も出にくくなる。
脳幹のモノアミン系神経病変はうつ等の精神症状の発現に関係するが、初期段階でNFTの残存する神経細胞数に対する出現頻度を調べてみると、青斑核(ノルアドレナリン系)で10〜20%、縫線核群(セロトニン系)では10〜15%であった。黒質神経細胞(ドパミン系)はニューロメラニンの存在のために観察し難いが、過マンガン酸カリで処理して観察したところではNFTの分布は少なかった(図10:Ishii T, Acta Neuropathol 6(1966)181-187)。参考に神経細胞脱落の程度をこれまでの報告に従って列挙すると、青斑核 (67〜81%の減少)、縫線核 (36%の減少)、視床背側前核 (80%の減少)である。これらの値は検索対象に選んだATDの病期によって異なるので互いに数値を比較するのは無意味であるが、全体の傾向を知るには有用である。
大脳白質では強く萎縮した皮質に対応する領域を中心に広範に髄鞘・軸索の脱落(図11B)と,これに伴う線維性グリオーシスがみられ萎縮しており、このために側脳室は拡大している。皮質下のU線維は保たれる傾向がある。ATDでは血管病変も合併していることが多く、そのような病態は特に混合型認知症(mixed-type dementia)と名付けられている。なかでも細動脈硬化性病変(いわゆるビンスワンガー型脳症)を伴う場合は、び漫性に高度の白質の萎縮が起こって来る。ATD自体の白質病変については、一つには皮質の神経細胞脱落に伴う軸索の変性〜脱落によるものと解釈される。しかしながら白質に一次性の病変が起こらない訳ではない。抗タウ免疫染色で観察すると白質の軸索にもタウ蛋白の蓄積が観察される(図11C)。
* SPが殆どみられず、NFTのみが出現する神経原線維型老年期認知症:SD-NFT) ではNFTの分布は海馬領域を中心とする辺縁系にとどまり、大脳新皮質には殆ど広がらない。SD-NFTは生理的加齢が進行した究極状態と考えられている。このことから海馬領域のNFT形成には加齢要因が働いていると考えられる。 すでに述べたように、ATDの大脳皮質の冒され方は一様ではない。 NFTのATD脳での広がり方には一定の空間的な法則があるように見える。皮質6層構造でみるとNFT好発層があり、V, VI層に最初に現れ、次いでIII層が好発層である。これらの層を構成する神経細胞は中〜大型の錘体細胞であり、錘体細胞は他の脳回や反対側の半球、あるいは皮質下の神経核を結ぶ長い線維である。すなわち、NFTは連合、交連、投射線維を出す細胞に出現しやすい。大脳新皮質でのNFT形成の空間的な進展について、視覚系を例にとって紹介しよう。視覚器からの情報は、外側膝状体→一次視覚野(ブロードマンの17野)→二次視覚野(18野)→三次連合野(19野*)→視覚連合野(20, 37野)へと伝達され、視覚情報は統合されてゆく。これをNFTの出現密度でみると、20, 37野に最も多く、次いで、18, 19野で、17野には少なく、外側膝状体にはNFTは出現しない(図12)。即ち、情報統合の上位の領域ほどNFT密度が高いという傾向があり、これは他の感覚情報系にも共通している。前述したようにATDでは髄鞘化の遅い領域(図2)、すなわち連合野でも上位の領域が強く冒される傾向がある。NFT分布から見たこのようなATD脳の冒され方はATDの認知症の特徴をよく説明する。
*19野を視覚連合野とする報告もある。
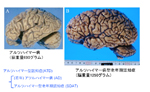
附記:海馬の嗅内野は最初にNFTが出現し、最も高度に冒される領域であるが、ここには脳の広範な領域からの感覚情報が集中して入力し、海馬へ出力する重要な中継点である。嗅内野と海馬の間には、嗅内野→海馬顆粒層→CA3, 4→CA1→海馬台→嗅内野、というサーキットが形成されている。これをNFT密度からみると、ほぼ、嗅内野>海馬支脚>CA1>CA3, 4の順であり、嗅内野から遠ざかるほどNFT密度が低いという階層傾向が認められる。そして、嗅内野へ感覚情報が入力し、出力するII層(pre-α)が最も早期に高度に冒され、次いで、大脳皮質、扁桃体やマイネルト神経核に出力するV層が冒されるという特徴が認められる。 図13は初老期発症のアルツハイマー病(A: AD, 早発性アルツハイマー病あるいは若年性アルツハイマー病とも言われる)と高齢発症のアルツハイマー型老年期認知症(B: SDAT, 晩発性アルツハイマー病とも言われる)である。両者を較べると、小脳がほぼ同じ大きさであるのに対して、大脳の萎縮には大きな違いがある。図12は筆者が経験したATD脳で最も萎縮が高度であった例と最も萎縮が軽度であった症例であるので、ATDの脳萎縮の両極端を示している。このように極端ではないにしてもADとSDATでは大脳の萎縮に大きな違いがある。海馬を通る前額断面で見てみるとADでは海馬領域を含めて、ほぼすべての脳回が萎縮しているのに対して(図14A)、SDATでは海馬傍回・海馬の萎縮は強いもののその他の皮質領域の萎縮は目立たない(図14B)。この相違は一般にADでは経過が速く高度の認知症に陥るのに対して、SDATは経過がゆっくりでADほど高度の認知症には陥らないとされる臨床に対応している。
このようにADとSDATでは脳萎縮に相違がある。萎縮領域には変性の項で述べたように、萎縮が高度の部位では全層性に、軽い部位では皮質上層に組織の粗しょう化〜海綿状態が起こる。海馬領域ではADとSDATでNFTの出現は接近しているが、大脳新皮質においてはADではSDATよりもはるかにNFTの出現頻度が高く数倍〜10倍程度の相違がある(図15)。NFTの出現の程度は萎縮の程度、すなわち神経細胞脱落の程度とほぼ一致している*。SPについても量的にはほぼ同様の傾向があり、ADではSDATよりも出現頻度が高いがNFTほどの量的な差はない(図16)。 このような結果、定型的なSDATではADのような皮質の組織の粗しょう化や、その結果としての強い萎縮は起こらない。そしてSDATはADと比較するとSPもNFTもより加齢脳に近い分布を示している。このようにADとSDATでは病理像に違いがある。それでは高齢者のATDではAD病像は起こらないのであろうか?
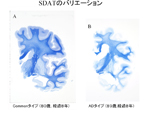
* NFTの出現の程度と分布は神経細胞脱落の程度と分布を反映しており、NFTは神経細胞脱落を知るよい指標である。 一般にはATDを発症年齢65歳で分け、65歳以前の発症のアルツハイマー病(AD)と、65歳以降の発症のアルツハイマー型老年期認知症(SDAT)と年齢で区別している。しかしながら、認知症の診療に従事する者であれば、高齢発症であっても経過が速く高度の認知症に陥る例が一定の割合で存在することを経験するはずである。この臨床での現象は室伏によりSDATのAlzheimerization(アルツハイマー化)と名付けられている。そのような症例の剖検脳を見ると、萎縮の様子は通常のSDATよりもADに近い(便宜上、ADタイプと呼ぶ)。通常のSDAT(便宜上、commonタイプと呼ぶ)では、前項で述たように、海馬領域を中心とする側頭葉内側低部に強い萎縮を示し、これを反映して側脳室下角が開大しているのに対して、新皮質領域の萎縮は軽い(図17A)。これに対して、ADタイプでは新皮質にも萎縮が認められ、初老期発症のAD(図14A)とほとんど区別がつかない(図17B)。顕微鏡で観察するとcommonタイプのSDATではNFTは海馬〜海馬傍回には多数認められるが、側副溝を越え、大脳新皮質に入ると急速に減少する。これに対して、ADタイプでは、側頭葉、島回、帯状回のいわゆる辺縁系皮質を中心に、新皮質にもIII層およびV, VI層にNFTが層状に分布しているのが観察される(図18)。これに比例して皮質II, III層、次いでV, VI層に神経細胞脱落と組織の粗鬆化(海綿状態)が認められ、その病理像は初老期発症のADと変わらない。このような初老期のADに匹敵する症例はSDATの約10%を占めている。このような症例 (ADタイプ) では、一様に認知症の進行が早く、4〜5年の経過で認知機能や言語機能が強く障害され、最終的には高度の認知症に陥る。巣症状も初老期のADほど目立たないがしばしば失語、失行などの巣症状が観察されるし、ケイレン発作を伴うことがある。このような事実は、老年期には加齢要因の強い通常のSDATが急増するが、変性性の強いADタイプも老年期に至っても初老期と変わらない割合で起こっているようである。ADタイプもcommonタイプも性質の同じ病理像(SP, NFT, 神経細胞脱落)を示すがゆえに「老年期発症のAD」は老年期に急増する通常のSDATの陰に隠れている(図19)。
これに関連して最後に、病変形成の速度と症状の発現について言及しておきたい。ATDに限ったことではないが、急速に病変が形成されるほど、その領域に関連した症状が強く現れやすい。同じ程度の病変があってもSDATよりもADで巣症状が現れやすい所以である。病変形成の速度は組織の反応の程度である程度類推できる。すなわち病変形成の時間的経過もある程度病理所見から類推することが可能である。